|
martes, 25 de septiembre de 2012
domingo, 23 de septiembre de 2012
Hipertrofia de adenoides
Es la inflamación del tejido linfático que se encuentra en la vía respiratoria entre la nariz y la parte posterior de la garganta. Este tejido es similar a las amígdalas.
Causas, incidencia y factores de riesgo
El agrandamiento de las vegetaciones adenoides puede presentarse de manera natural, comenzando cuando el bebé crece en el útero.
La inflamación prolongada también puede llevar a la hipertrofia de las adenoides.
Las vegetaciones adenoides normalmente se encogen a medida que el niño va creciendo.
Síntomas
- Mal aliento
- Labios cuarteados
- Resequedad en la boca
- Respiración bucal (principalmente en la noche)
- Boca abierta durante el día (en las obstrucciones más severas)
- Rinorrea o congestión nasal persistente
- Inquietud durante el sueño
- Ronquidos
Signos y exámenes
Las adenoides no se pueden visualizar por observación directa de la cavidad bucal, pero pueden verse con un espejo especial o mediante el uso de un endoscopio flexible a través de la nariz.
Los exámenes pueden incluir:
- Radiografía (vista lateral de la garganta)
- Estudios de la apnea del sueño (únicamente en los casos severos)
Tratamiento
Se pueden emplear antibióticos para tratar infecciones en las amígdalas, adenoides y senos paranasales cuando se presenten.
La extirpación quirúrgica de las adenoides (adenoidectomía) puede aliviar los síntomas o prevenir complicaciones en aquellas personas con infecciones auditivas o sinusales frecuentes o líquido detrás de los oídos. También se puede realizar cuando los tubos de timpanostomía no han reducido las infecciones de manera eficaz.
Expectativas (pronóstico)
Se espera una recuperación completa.
Complicaciones
- Frecuentes infecciones del oído
- Apnea del sueño intermitente
Situaciones que requieren asistencia médica
Consulte con el médico si su hijo presenta dificultad con la respiración a través de la nariz o si tiene otros síntomas de agrandamiento de adenoides.
Prevención
El tratamiento de las infecciones de la garganta en forma oportuna puede prevenir el agrandamiento de las adenoides a partir de una infección e inflamación prolongada. La extirpación de las adenoides previene la obstrucción prolongada de las vías respiratorias.
Nombres alternativos
Agrandamiento de las vegetaciones adenoides
Referencias
Wetmore RF. Tonsils and adenoids. In: Kliegman RM, Behrman RE, Jenson HB, Stanton BF, eds. Nelson Textbook of Pediatrics. 18th ed. Philadelphia, Pa: Saunders Elsevier; 2007:chap 380.
martes, 11 de septiembre de 2012
Botiquin de Viaje
Los siguientes artículos y medicamentos son una sugerencia para su viaje. Consulte con su médico posibles contraindicaciones de uso de algunos de los medicamentos. En caso de enfermedad, si los síntomas persisten debe consultar médico. Mantenga este botiquín fuera del alcance de los niños.• Algodón, gasa, tela adhesiva• Venda elástica• Termómetro• Povidona yodada, 1 frasco• Pomada antibacteriana: Dermabiótico, 1 tubo• Antialérgico: Loratadina (ClarityneR) 1 caja
• Antipirético y analgésico: Paracetamol 500 mg, 1 caja
• Antinflamatorio: Ibuprofeno 400 mg, 1 caja
• Antidiarreico: Loperamida (CapentR) 2 mg, 1 caja
• Sales de rehidratación: RehSal 60, 1 caja• Antipruriginoso: Caladryl, 1 frasco. Aplicar en área afectada 3 veces al día• Bloqueador solar, factor 25-30
lunes, 3 de septiembre de 2012
Dolor de la articulación sacroilíaca. Anatomía, Diagnóstico y Tratamiento
Revista de la Sociedad Española del Dolor
versión impresa ISSN 1134-8046
Rev. Soc. Esp. Dolor v.15 n.3 Narón (La Coruña) abr. 2008 REVISIONES
Sacroiliac joint pain. Anatomy, Diagnosis and Treatment
G. E. Mejía1, M. Arias2, K. Valdez3, S. Carrillo2, G. Infante21Médico Anestesiólogo-Algologo. Jefe de la Clínica del Dolor del Instituto Nacional de Rehabilitación. 2Médico Anestesiólogo-Algologo. Adscrito al Servicio de Clínica del Dolor del Instituto Nacional de Rehabilitación. 3Médico Ortopedista. Adscrita al Instituto Nacional de Rehabilitación.
RESUMEN
El dolor de la articulación sacroilíaca es una causa frecuente de dolor bajo de espalda, sin embargo el diagnóstico de artralgia sacroilíaca no es fácil de confirmar y la exploración física de la articulación es controvertido. Además este diagnóstico a menudo pasa inadvertido para el médico, por lo que la falta de consideración de esta posible causa de lumbalgia da lugar a tratamientos inapropiados e inadecuados. La articulaciones sacroilíacas, sinoviales del tipo anfiartrosico irregular, monoaxiales, en la cual se articulan las carillas articulares del sacro al ilion, Su innervación es cuestión de debate, pero las más recientes investigaciones refieren que deriva de L2-S2, L4-S2, L5-S2. La prevalencia del dolor de la articulación sacroilíaca no esta bien estudiado, hay numerosas etiologías para el dolor de articulación sacroilíaca, estas causas se pueden dividir en intraarticulares y extraarticulares. Para la exploración física se cuenta con una serie de 12 pruebas las cuales fueron emitidas por un comité de expertos y se concluye que encontrar 3 o más pruebas positivas es muy sugestivo de dolor de dicha. El tratamiento se puede dividir en conservador, intervencionista donde se puede utilizar desde la infiltración con anestésico local y esteroide hasta radiofrecuencia y por ultimo quirúrgico para casos seleccionados.
Palabras clave: Dolor, articulación sacroilíaca, dolor articulación sacroilíaca.
SUMMARY
The pain of the sacroiliac joint is a frequent cause of low back pain, however the diagnose of sacroiliac artralgia it is not easy to confirm and the physical exploration of the joint is controversial. Also this I often diagnose it happens inadvertent for the physician, for what the lack of consideration of this possible low back pain cause gives place to inappropriate and inadequate treatments. The sacroiliac joint is synovial of the type irregular anphiarthrosic, monoaxial, in which the sides joint are articulated from the sacrum one to the Ilion, Their innervation is debate question, but those but recent investigations refer that it derives of L2-S2, L4-S2, L5-S2. The prevalence of the pain of the sacroiliac joint not this well studied one, there is numerous etiology for the sacroiliac joint pain, these causes can be divided in intraarticular and extraarticular. For the physical exploration it is had a series of 12 tests which were emitted by a committee of experts and you concludes that to find 3 or but positive tests are very suggestive of pain of happiness. The treatment you can divide in conservative, interventionist where you can use from the infiltration with local anesthetic and steroid until radiofrequency and for finish surgical for selected cases.
Key words: Pain, Sacroiliac joint, Sacroiliac joint pain.
Introducción
El dolor de la articulación sacroilíaca (ASI) es una causa frecuente de dolor bajo de espalda, sin embargo el diagnóstico de artralgia sacroilíaca no es fácil de confirmar y la exploración física de la articulación es controvertido. Además este diagnostico a menudo pasa inadvertido para el médico, por lo que la falta de consideración de esta posible causa de lumbalgia da lugar a tratamientos inapropiados e inadecuados.
Anatomía
Estructura Articular: La articulaciones sacroilíacas, sinoviales del tipo anfiartrosico irregular (1,2,3), monoaxiales, en la cual se articulan las carillas articulares del sacro al ilion, están cubiertas de un cartílago articular parecido al fibrocartílago y fibras delgadas ínteróseas, contiene asimismo líquido sinovial; en las que se presentan elevaciones y depresiones irregulares permitiendo la unión parcial de ambos huesos, (4,5). Presenta una movilidad limitada (4 grados de movimiento y 1.6 mm de traslación total) (6).
Ligamentos: Los ligamentos que mantienen esta estrecha unión son para la región profunda: Los iliolumbares que consta de dos haces el superior y el inferior. Los ligamentos iliosacros, el iliotransverso sacro, los iliotransverso conjugados que son un complejo formado por 4 ligamentos, el primero va de la tuberosidad iliaca al primer tubérculo conjugado, (5,7,8) el de Zaglas que se fija al segundo tubérculo, el tercero y cuarto se extienden de la espina iliaca posterosuperior a los tubérculos conjugados tercero y cuarto (4,7,8,9). En la parte inferior del borde externo del sacro y la gran escotadura ciática se extienden los ligamentos sacro ciáticos mayor y menor; el primero es oblicuo hacia arriba de adentro hacia atrás, desde la espina ciática al borde lateral del sacro y el cóccix; el segundo atraviesa con haces oblicuos la cara posterior, se inserta en el borde posterior del iliaco a las dos primeras vértebras coccígeas, por abajo en la tuberosidad isquiática (7,10,11). La gran escotadura ciática se halla dividida por estos dos ligamentos sacrociáticos, el orificio superior por el que sale de la pelvis el músculo piramidal y el orificio inferior que es la salida del obturador interno. El ligamento axial (interoseo o vago) se fija por fuera en la tuberosidad iliaca y por dentro en las dos fosas cribosa del sacro, representa el eje en el cual se ejecutan los movimientos del sacro (4,7,9) (Fig. 1 y 2).
Irrigación: La irrigación de las articulaciones sacro ilíacas es por parte de las arterias glúteas superior, iliolumbar y sacral lateral.
Inervación: Su inervación es cuestión de debate, pero las más recientes investigaciones refieren que deriva de L2-S2, L4-S2, L5-S2 (12). Los estudios de neurofisiología han identificado que presenta un total de 29 unidades mecanosensitivas, de estas 26 están ubicadas en la cápsula y 3 se ubican adyacentes a los músculos, 28 son nociceptores y 1 es propioceptivo (13).
Función: La función de estas articulaciones es dar soporte al esqueleto axial, así como facilitar el parto, se diferencian de la mayoría de las articulaciones sinoviales por que tienen poca movilidad, lo que explica su estabilidad. Debido a que la unión articular es irregular el acoplamiento es seguro y no resulta fácil su luxación. El movimiento de nutación fue descrito por Zaglas y Duncan, en el cual el sacro gira en torno al eje del ligamento axial, de tal modo que el promontorio se desplaza hacia abajo y adelante, mientras que el vértice del sacro y el cóccix se desplazan hacia atrás (7,11). Las alas iliacas se aproximan mientras las tuberosidades isquiáticas se separan, en este movimiento, la contra nutación, se presenta de forma inversa, el sacro a pivotar en torno al ligamento axial, se endereza, el promontorio se desplaza hacia arriba y atrás, las alas iliacas se separan y las tuberosidades isquiáticas se aproximan, este movimiento esta limitado por la tensión de los ligamentos sacroilíacos de ambos planos tanto superficial como profundo. Por lo tanto cada ala del iliaco funciona como brazo de palanca, con vértice de apoyo en la articulación sacro ilíaca, con resistencia y potencia en los extremos superiores e inferiores (4,7,14). El movimiento de la articulación sacroilíaca se limita a un desplazamiento mínimo y a un momento de rotación, salvo cuando se aplica un fuerza considerable o carga axial, por lo tanto la fuerza se transmite a partir de la columna vertebral (9,10,5,8) y se disipa al anillo pélvico, esta rotación es contrarrestada por los ligamentos de soporte que distribuyen la fuerza a los huesos iliacos y a las extremidades (1,2,3,15).
Epidemiología
Basado en historia clínica y examen físico, la epidemiología del dolor de articulación sacroilíaca puede ser reportado con presencia de síntomas del lado derecho en un 45% de los casos, del lado izquierdo en un 35% y bilateralmente en un 20%, con prevalencia de 22.5% de 62.8% (16,17). Más recientes investigadores intentaron establecer la prevalencia de dolor de articulación sacroilíaca utilizando diagnóstico por fluoroscopia guiada con inyección intraarticular, reportando que la prevalencia de dolor crónico bajo de espalda ocasionado por articulación sacroilíaca es del 13-30% (17,18,19) Chout et al, (18) observaron retrospectivamente en 54 pacientes con dolor de la articulación sacroilíaca para encontrar la prevalencia de la causas que lo provocaron encontraron: traumatismo 44%, lesión repetitiva 21%, idiopático 35% de los cuales el (50%) contaba con antecedente de cirugía lumbar (17,18).
Etiología
La prevalencia del dolor de la articulación sacroilíaca no esta bien estudiado, mecánicamente, hay numerosas etiologías para el dolor de articulación sacroilíaca. Para simplificar, estas causas se pueden dividir en intraarticulares y extraarticulares (11).
Extra-articular: Las causas más comunes incluyen, enteropatías, fracturas, daño ligamentario y dolor miofascial.
Intraarticular: Infecciones y artritis (causas más comunes) (11,20).
En adición a las causas etiológicas, existen numerosos factores que pueden predisponer a una persona para desarrollar gradualmente dolor de articulación sacroilíaca. Factores de riesgo que funcionan incrementando la tensión llevada a la articulación son: la discrepancia verdadera y evidente de la longitud de las extremidades inferior, anormalidades de la marcha, prolongado ejercicio vigoroso, escoliosis, y fusión espinal del sacro (11,21).
Se han descrito así mismo factores que se presentan por incremento de la fuerza en la articulación tales como: ligamento debilitado por violación de la cavidad durante cirugía para toma de injerto de hueso iliaco, hipermovilidad post-quirúrgica (Tabla I).
El embarazo predispone a dolor en la articulación por diversos factores como son el incremento de peso, exagerada postura de lordosis, trauma durante el parto y laxitud ligamentaria inducida por hormonas, atribuida a incremento en los niveles de estrógenos y relaxina (11,22). La inflamación de una o ambas articulaciones sacroilíacas es considerada como un síntoma temprano e importante en todos los seronegativos y espóndiloartropatías asociadas a HLA-B27. Si bien la etiología precisa de la las espóndiloartropatías continua desconocida en la mayoría de los pacientes la fuerte asociación con HLA-B27 sustenta el punto de vista de que estas condiciones son atribuibles a una respuesta inmune determinada genéticamente a factores ambientales en individuos susceptibles. Otras etiologías son: infección, tumores malignos, lesiones deportivas, lesión por accidente automovilístico, torsión forzada, ascensos con pendientes pronunciadas (23).
Presentación clínica
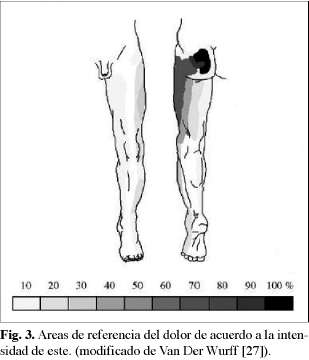
Semiológia del dolor: Los pacientes presenta dolor localizado alrededor de la articulación cuyo núcleo se encuentra en la espina iliaca posterosuperior y el trocánter mayor, no supera la línea del cinturón, es más común la presentación unilateralmente que la bilateral con una relación de 4:12 (24), se irradia a la nalga y a la región dorsal de la extremidad inferior, pero no alcanza la región de la rodilla, generalmente la actividad física lo empeora, así como los movimientos de transición como ponerse de pie desde la sedestacion o los movimientos bruscos inesperados, o pisar en superficies irregulares, yacer en posición de decúbito dorsal, esencialmente todos aquellos movimientos que generen movilidad de la región lumbar y la pelvis van a exacerbar el dolor debido al incremento del esfuerzo que estas actividades presentan sobre la articulación sacroilíaca (25). Fortín (26) describió una zona de irradiación de aproximadamente 3 x 10 cm justo inferior a la espina iliaca posterosuperior la cual la interpreta como específica de dolor generado en la articulación sacroilíaca, Van Der Wurff (27) en su estudio identifica las áreas de referencia del dolor de acuerdo a la intensidad de este, los cuales están dados por la zonas de inervación dermatómica de la articulación donde queda indemne el área de la tubérosidad isquiática (Fig. 3). El dolor disminuye al sentarse debido a la relajación de los músculos isquiotibiales (25). El tipo de dolor generalmente referido es de tipo sordo, quemante y opresivo, que puede convertirse en algo semejante a una puñalada, con una duración desde segundos hasta varios minutos en cada episodio de exacerbación, además de presentar un dolor basal pulsátil y persistente (25).
Exploración Física: Para la exploración física se cuenta con una serie de 12 pruebas las cuales fueron emitidas por un comité de expertos y se concluye que estas son las que más pueden tener especificidad para el dolor de la ASI (28) (Tabla II) Consisten en lo siguiente: La prueba de Gillet se realiza en el paciente de pie y las piernas separadas por unas 12 pulgadas aproximadamente, se palpa el proceso espinoso de S2 y las espina iliaca posterosuperior se pide al paciente que eleve la pierna como si fuera a dar un gran paso, la prueba resulta positiva si no se desplazan de la misma forma ambas estructuras. La prueba de compresión pélvica esta se realiza colocando las manos sobre las crestas iliacas y los pulgares sobre las espinas iliacas anterosuperiores se comprime la pelvis hacia la línea media, se considera positiva si produce dolor alrededor de la ASI. La prueba de Patrick/FABER en la que el paciente en posición de supino con la rodilla y cadera flexionada a 90º a continuación se coloca el pie sobre la rodilla contralateral en esta posición el examinador desplaza lentamente el muslo en un movimiento de abducción, y rotación externa se considera positiva si presentad dolor en la región de la ASI, La prueba de Gaenslen donde el explorador se coloca de pie detrás del paciente, hiperextiende la pierna de la articulación sacroilíaca examinada al tiempo que estabiliza la pelvis con la otra mano si se presenta dolor a nivel ASI se considera positiva, La prueba del flamenco donde se pide al paciente que se sostenga en un pie del lado afectado se le solicita que salte, el dolor en la región de la ASI indica una prueba positiva. La prueba de "juego articular" se realiza colocando las manos cruzadas sobre el sacro, la primera en la parte alta de la articulación y la segunda sobre el piriforme se aplica fuerza y se percibe el movimiento de la articulación lo que la considera positiva, se evalúan ambos lados. La prueba del empujón del muslo consiste en aplicar tensión a la articulación a través de la rotación del fémur (25).
Dreyfuss (29) concluye en su estudio que ninguna por si sola tiene un valor diagnóstico especifico. Broadhurst (30) demostró que tres pruebas clínicas positivas o más son de un alto valor predictivo de dolor de la ASI.
Estudios Radiográficos: La artrografía de la ASI puede descubrir las anormalidades en la morfología capsular, esto abarca áreas atenuadas discontinuas, rupturas, lágrimas francas y divertículos, que pueden variar en el tamaño, la forma y el número. La comunicación entre la ASI y los nervios que se encuentran a su alrededor pueden quizás explicar el dolor de carácter radicular. Las radiografías simples así como la tomografía computada son eficaces para valorar la normalidad o la morfología aberrante de la articulación. La radiografía simple es muy óptima para visualizar divertículos, mientras la TAC es superior para identificar lágrimas anteriores, extravasación y comunicaciones a otras estructuras. Se debe de considerar que la presencia de alteraciones estructurales en la articulación no asegura la presencia de alguna condición dolorosa (31).
Diagnóstico diferencial: El dolor de la ASI se confunde a menudo con el esquince lumbar, bursitis lumbar, fibromiositis lumbar, artritis, y trastornos de los nervios, plexos y medula espinal lumbar. Se deben de obtener imágenes radiológicas y de resonancia magnética de columna lumbar para descartar estas patologías. El dolor de la ASI se diferencia del dolor lumbar pidiendo al paciente que se incline hacia delante mientras esta sentado el dolor lumbar va a aumentar con esta prueba (25).
Tratamiento
Conservador: El tratamiento conservador debe incluir la aplicación de frío local, medicamentos Antiinflamatorios y reposo relativo en la etapa aguda. En cuanto el dolor ha disminuido, todos los esfuerzos debe estar empleados para restituir la normalidad mecánica, incluyendo: técnicas de medicina manual, la estabilización pélvica a través de ejercicios para obtener control postural dinámico y reforzar el equilibrio del tronco y las extremidades inferiores (32).
Fisioterapia y ejercicios: No existen estudios prospectivos que valoren el efecto de la fisioterapia, el ejercicio aeróbico, los ejercicios de estabilización o la restauración del alcance de movimiento en el síndrome de la articulación sacroilíaca (33). Sin embargo, el ejercicio es un aspecto importante en el tratamiento de este síndrome, al mismo tiempo que la estabilización aunque de manera empírica (34). Las estrategias que la fisioterapia proporciona se enfatizan en la estabilización pélvica, la restauración postural y dinámica originadas por debilidad de músculos, lo que origina anormalidades en la marcha. Varios autores han descrito desbalances musculares en pacientes con disfunción de la articulación sacroilíaca (ASI). Ésta debilidad se extiende desde el tronco hacia la extremidad baja a los músculos que refuerzan o relajan a la articulación sacroilíaca.
Este proceso puede involucrar una multitud de músculos, incluyendo al iliopsoas, cuadrado lumbar, piriforme, glúteo mayor y a los ligamentos tensores de la pelvis y quitar fuerza de músculos dinámicos incluyendo glúteo mayor, transverso abdominal y transverso espinoso (33,34). En el caso que se detecte este desbalance, un programa de fisioterapia se concentrara en estirar y fortalecer los músculos débiles, siendo este un importante elemento en el tratamiento de la ASI (32,33).
Aparatos Ortopédicos: Son varios los autores que defienden el uso de prótesis ortopédicas en el tratamiento de la ASI. Sin embargo, similar a otras modalidades de tratamiento no existen estudios controlados que valoren la eficacia de estos. Comúnmente el uso de prótesis ortopédicas se indica para favorecer la estabilización pélvica, intentar limitar el movimiento de la articulación y mejorar la propiocepción (33,34,35).
Terapia manual o quiropráctica: La terapia manual ha sido defendida comúnmente como un medio de tratamiento de la disfunción de la ASI y la estabilización. Sin embargo, Tullberg y cols mostró que la manipulación no modifica la posición del sacro en relación con el ilion. Aunque algunos estudios a favor sugieren beneficios asociados a esta (33,36,37).
Manejo Intervencionista: Si el tratamiento conservador falla, la inyección de anestésicos locales y un corticoesteroide debe ser considerado. No solamente como una intervención terapéutica, también para confirmar el diagnóstico. La reproducción de los síntomas por sobredistención de la cápsula articular y/o la atenuación de los síntomas por el bloqueo analgésico son los medios más confiables y reproducibles, por lo cuál el generador del dolor puede ser identificado (32). La selección debe ser reservada para los pacientes que no han respondido al tratamiento conservador o en quiénes han llegado a un período de estancamiento insatisfactorio. En estos casos, la inyección en la Articulación Sacroilíaca puede reduciendo el dolor y facilitando la rehabilitación (32). Para optimizar el diagnóstico y la seguridad terapéutica el uso de Fluoroscopia debe ser empleado. Las inyecciones a "Ciegas" son inexactas para llegar al espacio intraarticular. Hansen (38) en su estudio, involucraron a experimentados intervencionistas ha efectuar inyecciones en la ASI sin fluoroscopia. La orientación fue exitosa solamente en el 12 % de los 60 pacientes. Rosenberg (39) en su estudio demuestra también una baja tasa de éxitos además de demostrar bajo tomografía computada la extravasación de medio de contraste fuera de la articulación así como la diseminación hacia los forámenes sacros e incluso aplicación en espacio epidural.
Técnica: Bajo la orientación con fluoroscopia, una aguja vertebral calibre 22 o 25 de ancho y largo de 3.5 pulgadas. Se infiltra piel y tejidos subcutáneos Lidocaína al 1%. Se utiliza medio de contraste no iónico (por ejemplo, Iohexol o iopamidol) (32). Son varios los agentes anestésicos y esteroides que se pueden aplicar desde lidocaína o bupivacaina, combinada con hidrocortisona, betametasona, triamcinolona o metilprednisolona. El paciente es colocado en decúbito prono, se procede a la asepsia y la colocación de campos estériles. La aguja es dirigida hacia la región inferior de la articulación sacroilíaca, con una visión posteroanterior (PA) directa. El sitio acostumbrado de entrada es el tercio inferior de la articulación dónde un espacio radiolucido debe admitir el paso de la aguja con resistencia mínima. Puede haber dos o más "ramas" de la articulación, porque la articulación es lateralmente divergente de su parte posterior para los bordes anteriores y puede haber ínterdigitaciones. Se recomienda primero visualizar adecuadamente el espacio intervertebral de L5-S1 ajustando la visión ya sea cefálica o caudal, posteriormente se rota a una visión anteroposterior y en oblicuo se procede a visualizar la articulación, al girar el brazo en C de manera oblicua debe permitir una perspectiva tridimensional de la articulación y permitir la selección de la "Ventana" para una trayectoria de la aguja óptima. Una vez que se atraviesan los ligamentos sacroilíacos e interoseos dorsales, la aguja adopta a menudo una curva característica porque se ajusta a los contornos de la articulación (32,40).
Este fenómeno es a menudo precedido por una impresión táctil sutil de disminución de la resistencia una vez que se penetra el ligamentos y entra en la articulación. Si la resistencia es mayor o se cree que se esta chocando con hueso se debe retraer ligeramente la aguja y girar el bisel hacia el espacio interarticular lo que desviará la aguja y la ajustara a los márgenes de la misma (40) (Fig. 4). La administración de medio de contraste debe dibujar una forma semejante al borde de una moneda en la visión anteroposterior (AP) y se produzca la forma de "oreja" en la visión oblicua lo que confirmaría la correcta colocación de la aguja.
Las respuestas a la provocación producen un dolor intenso en la región glútea producto de la estimulación de una ASI sintomática (31). Para las inyecciones analgésicas. La capacidad volumétrica de la ASI es de 3 a 5 ml como máximo por lo tanto, se deben ajustar los volúmenes para el anestésico y el corticosteroide (31).
Radiofrecuencia: Para el caso en que se desea realizar la denervacion con radiofrecuencia, la técnica es la misma y una vez que están colocadas la agujas, se realiza prueba de estimulación sensitiva y motora, se recomienda una aguja de 100mm o 145mm con una punta activa de 0.5 a 1.0 cm (40). Los parámetros de estimulación sensitiva son a 50Hz con una potencia hasta 1 V, una prueba positiva se obtiene al referir parestesia al estímulo en 0.5 V o más. Ya que se descartó estimulación a alguna estructura motora cercana, se procede a realizar la lesión, se inyecta 1ml de Lidocaína al 2% y se inicia el ciclo a 80ºC por 90 segundos. Se deben realizar múltiples lesiones a lo largo de toda la cara posterior de la articulación. Es recomendado aplicar radiofrecuencia a las facetas y al ganglio de la raíz dorsal para brindar un tratamiento completo, la aplicación de radiofrecuencia pulsada al ganglio de la raíz dorsal de S1, S2, S3 y radiofrecuencia continua a las ramas medias de L4 y L5 es lo más adecuado, una rama segmentaría de la raíz de S2 contribuye de manera importante a la inervación de la ASI de tal manera que la radiofrecuencia pulsada al ganglio de la raíz dorsal de S2 alivia los síntomas residuales a la denervacion de la articulación. Posterior a la denervacion con radiofrecuencia algunos pacientes llegan a presentar molestias en el área del glúteo, dolor pélvico o dolor referido a la cara posterior del muslo, que resuelve en 10 a 15 días, de manera que la terapia analgésica oral se debe ajustar a estas necesidades, una área de hipoestesia en el glúteo también puede ser referida por el paciente, la cual resuelve espontáneamente en 2 a 4 semanas (40). Aunque se han descrito periodos de alivio por más de 6 meses en varios artículos, no existe muchas referencias que soporten a la radiofrecuencia como el tratamiento estándar, por lo que se deben de realizar estudios prospectivos a largo plazo así como de costo-beneficio que sustenten la eficacia de la radiofrecuencia en esta patología (41,42).
Crioneuroablación: La crioneuroablación, también conocida como crioanalgesia o crioneurolisis, es una técnica especializada que provee mejoría del dolor a largo plazo y forma parte importante dentro del armamento terapéutico intervencionista del dolor. La crioanalgesia moderna obtiene sus raíces desde que Cooper y cols desarrollan en 1961 un dispositivo que usaba nitrógeno líquido a través de un tubo hueco con la punta sin aislamiento, con lo que se obtiene una temperatura de -190ºC. Posteriormente Lloyd y cols. lo proponen como un dispositivo periférico superior a otras técnicas neurodestructivas, como la neurolisis por alcohol, fenol o quirúrgicas (43). La aplicación de frío en el tejidos nervioso causa un bloqueo de la conducción similar al efecto de los anestésicos locales. El alivio del dolor a largo plazo con la congelación de los nervios ocurre debido a que los cristales de hielo generan lesión a la vasa nervorum, lo que produce edema endoneural grave. La crioanalgesia afecta la estructura nerviosa creando degeneración Walleriana; pero sin dañar la vaina de mielina y dejando al endoneuro intacto (43). Para el procedimiento de crioneuroablación, el paciente es colocado en decúbito prono y el foramen del sacro a tratar identificado con fluoroscopia. Después de preparar la zona a abordar, se infiltra una pequeña cantidad de anestésico local en piel y tejido subcutáneo profundo, entonces se infiltra una pequeña cantidad de solución salina con epinefrina (1:200,000) aproximadamente 1 ml. Después de que un pequeño corte en la piel es hecho, el introductor calibre 12 es colocado hasta el borde inferior del foramen de manera lateral. El estilete es retirado y se introduce la sonda de 2.0 mm por el catéter. Se usa un estímulo doloroso para identificar el área con mayor dolor. Se debe de tener cuidado de no entrar en el foramen dado que por la inervación de las ramas sacras se puede dañar potencialmente los nervios que controlan el intestino y la vejiga. Aunque existen estudios que apoyen el uso de la crioanalgesia, debe ser aplicado por clínicos con experiencia, respecto al costo beneficio del procedimiento los resultados aun no han sido publicados (43).
Guía ultrasonógráfica: En un afán por disminuir la exposición a los rayos X se puede guiar la infiltración de articulación a través de un equipo de ultrasonógráfica para lo cual utilizamos un transductor recto, colocado en posición transversa, se ubica la línea media sobre el proceso espinoso del sacro y aproximadamente a 5 cm lateral a esta con un rango de 3.5 a 6 cm se ubica la articulación, vamos a obtener una imagen hiperecoica de forma lineal la cual representa al iliaco y más lateralmente al sacro entre ambas imágenes se observa una zona hipoecoica la cual es la ASI. Una vez localizada se introduce la aguja hasta el tercio distal de la misma, lugar donde se deposita el anestésico y esteroide (44) (Fig. 5).
Quirúrgico: La fijación quirúrgica de la ASI se realiza en aquellas articulaciones altamente inestables. Se asume que la estabilización reducirá el dolor y la incapacidad, aunque esto no esta totalmente comprobado. Solo que la etiología sea traumática o cualquier otra que este relacionada con debilidad ligamentaria de la ASI puede verse beneficiada con este procedimiento quirúrgico pero no debe de ser un procedimiento de rutina en el tratamiento.
Son varios los reportes en los que se comentan beneficios que van desde un 50% a un 90% de alivio del dolor. No todos los pacientes requerirán de cirugía para obtener mejoría y se debe de considerar como una de las últimas alternativas de tratamiento (32,33,45,46).
Bibliografía
1. Rosatelli A Agur A Chhaya S Anatomy of the Interosseous Region of the Sacroiliac Joint J Orthop Sports Phys Ther 2006: 36: 200-8. [ Links ]
2. Cibulka M, Sinacore D, Cromer G, Delitto A Unilateral hip rotation range of motion asymmetry in patients wifh sacroiliac joint regional pain. Spine. 1998; 23: 1009-15. [ Links ]
3. Grgic V The sacroiliac joint dysfunction: clinical manifestations, diagnostics and manual therapy Lijec Vjesn. 2005; 127: 30-5. [ Links ]
4. Zelle B, Gruen G, Brown S, George S. Sacroiliac joint dysfunction: evaluation and management. Clin J Pain. 2005; 21: 446-55. [ Links ]
5. Fortin J, April C, Ponthieux B, Pier J. Sacroiliac joint: pain referral maps upon applying a new injection/arthrography technique. Part II: Clinical evaluation. Spine. 1994; 19: 1483-9. [ Links ]
6. Akuthota V Willick S Harden N La columna vertebral del adulto: enfoque practico del dolor lumbar. En Rucker K Cole A Weinstein S Dolor Lumbar McGraw Hill Madrid España 2003 p 19-50. [ Links ]
7. Harrison D, Harrison D, Troyanovich SJ. The sacroiliac joint: a review of anatomy and biomechanics with clinical implications. J Manipulative Physiol Ther. 1997: 20: 607-17. [ Links ]
8. Brolinson G, Kozar J, Cibor G. Sacroiliac joint dysfunction in athletes. Curr Sports Med Rep. 2003: 2: 47-56. [ Links ]
9. Daum W The sacroiliac joint: an underappreciated pain generator. Am J Orthop. 1995; 24: 475-8. [ Links ]
10. Foley B, Buschbacher R Sacroiliac joint pain: anatomy, biomechanics, diagnosis, and treatment Am J Phys Med Rehabil. 2006: 85: 997-1006. [ Links ]
11. Cohen S. Sacroiliac joint pain: a comprehensive review of anatomy, diagnosis, and treatment. Anesth Analg. 2005: 101: 1440-53. [ Links ]
12. Ikeda R Innervation of the sacroiliac joint macroscopic and histological studies J Nipppon Med Sch 1991: 58: 587-96. [ Links ]
13. Sakamoto N Yamashita T Takebayashi T An electrophysiologic study of mechanoreceptors in the sacroiliac joint and adjacent tissues Spine 2001: 26; E 468-71. [ Links ]
14. Cibulka M, Koldehoff R Clinical usefulness of a cluster of sacroiliac joint tests in patients with and without low back pain J Orthop Sports Phys Ther. 1999: 29: 83-9. [ Links ]
15. Toussaint R, Gawlik C, Rehder U, Ruther W. Sacroiliac dysfunction in construction workers. J Manipulative Physiol Ther. 1999; 22: 134-8. [ Links ]
16. Goldthwaite G, Osgood R. A consideration of the pelvis articulation from an anatomical, pathological, and clinical standpoint. Boston med Surg J. 1905; 152: 593-601. [ Links ]
17. Slipman C, Whyte W, Chow D, Chou L, Lenrow D, Ellen M. Sacroiliac join syndrome. Pain Physician. 2001: 4: 143-152. [ Links ]
18. Chout L, Slipman C, Bhagia S, Tsaur L, Bhat AL, Isaac Z, Gilchrist R, El Abd OH, Lenrow Da. Inciting event initiating injectionproven sacroiliac joint syndrome. Pain Med. 2004: 5: 26-32. [ Links ]
19. Burnham R, Yasui Y. An alternate method of radiofrecuency neurotomy of the sacroiliac joint: a pilot study of the effect on pain, function, and satisfaction. Reg Anesth Pain Med. 2007: 32: 12-19. [ Links ]
20. Luukkainen R, Wennerstrand P, Kautiainen H, Efficacy of periarticular corticosteroid treatment of sacroiliac joint in non-spondyloarthropathic patients with chronic low back pain in the región of the sacroiliac joint. Clin Exp Rheumatol. 2002; 20: 52-4. [ Links ]
21. Katz V, Schofferman J, Reynolds J. The sacroiliac joint: a potential cause of pain after lumbar fusion to the sacrum. J Spinal Disord Tech. 2003; 16: 96-9. [ Links ]
22. Albert H, Godskesen M, Westergaard J. Prognosis in four syndromes of pregnancy-related pelvic pain. Acta Obstet Gynecol Scand. 2001; 80: 505-10. [ Links ]
23. Cohen S Epidemics evolution and sacroiliac joint pain Reg anest pain med 2007: 32: 3-6. [ Links ]
24. Prather H Hunt D conservative management of low back pain part I sacroiliac joint pain Dis Mon 2004: 50: 670-83. [ Links ]
25. Waldman S Dolor en la articulación sacroilíaca En: Waldman S Atlas de síndromes dolorosos frecuentes Elservier-Saunders Madrid España 2003 p 212-15. [ Links ]
26. Fortin J, April C, Ponthieux B, Pier J. Sacroiliac joint: pain referral maps upon applying a new injection/arthrography technique. Partí: aymmptomatic volunteers. Spine. 1994; 19: 1475-82. [ Links ]
27. Van Der Wurff P Buijs E Groen G. Intensity mapping of pain referral areas in sacroiliac joint pain patients Journal of manipulative ad physiological therapeutics 2006: 29: 190-95. [ Links ]
28. Waldman S Exploración física de la Cadera En: Waldman S Atlas diagnóstico del dolor un enfoque por signos y síntomas Elservier-Saunders Madrid España 2007 p 281-319. [ Links ]
29. Dreyfuss P Michaelsen M Pauza K McLarty J Bogduk N The Value of Medical History and Physical Examinad on in Diagnosing Sacroiliac Joint Pain Spine1996: 21: 2594-2602. [ Links ]
30. Broadhurst N Bond M Pain provocation test for the assessment of sacroiliac joint dysfunction J Spinal Disord 1998: 11: 341-5. [ Links ]
31. Fortin JD,Vilensky JA,Merkel GJ. Can the Sacroiliac Joint Cause Sciatica?. Pain Physician. 2003; 6: 269-271. [ Links ]
32. Forst SL, Wheeler MT, DO, Fortín JD, Vilensky JA. The Sacroiliac Joint: Anatomy, Physiology and Clinical Significance. Pain Physician. 2006; 9: 61-68. [ Links ]
33. Hansen HC, Helm II S. Sacroiliac joint pain and dysfunction. Pain Physician. 2003; 6: 179-189. [ Links ]
34. Slipman CW, Whyte II WS, Chow DW, Chou L, Lenrow D, Ellen M. Sacroiliac joint syndrome. Pain Physician. 2001; 4: 143-152. [ Links ]
35. Cibulka, MT, Koldehoff RM. Leg length disparityand its effect on sacroiliac joint dysfunction. Clinical Management. 1986; 6: 10-11. [ Links ]
36. Osterbauer PJ, Deboer KF, Widmaier R. et al. Treatment and biochemical assessment of patients with chronic sacroiliac syndrome. J Manipulative Phys Ther. 1993; 16: 82-90 [ Links ]
37. Tullberg T, Blomberg S, Branth B et al. Manipulación does not alter the position of the sacroiliac joint, A roentgen stereophotogrammetric analysis. Spine 1999; 23: 1124-1128. [ Links ]
38. Hansen HC. Is Fluoroscopy Necessary for Sacroiliac Joint Injections?. Pain Physician. 2003; 6: 155-158. [ Links ]
39. Rosenberg JM, Quint TJ, de Rosayro AM. Computerized tomographic localization of clinically-guided sacroiliac joint injections. Clin J Pain. 2000; 16: 18-21. [ Links ]
40. Raj PP Luo L. Erdine S. Staats PS. Waldman SD. Radiographic imaging for regional anesthesia and pain management. Churchill Livingstone. USA. 2003. 242-44. [ Links ]
41. Hansen HC, McKenzie-Brown AM, Cohen SP, Swicegood JR, Colson JD, Manchikanti L. Sacroiliac Joint Interventions: A Systematic Review. Pain Physician. 2007; 10: 165-184. [ Links ]
42. McKenzie-Brown AM, Shah RV, Sehgal N, Everett CR. A Systematic Review of Sacroiliac Joint Interventions. Pain Physician. 2005; 8: 115-125. [ Links ]
43. Trescot AM. Cryoanalgesia in Interventional Pain Management. Pain Physician. 2003; 6: 345-360. [ Links ]
44. Pekkafali M Zeki M Cihat 3inar Silit E Mutlu H Óz-türk E Kizilkaya E Dursun H Sacroiliac Joint Injections Performed With Sonographic Guidance J Ultrasound Med 22: 553-559, 2003. [ Links ]
45. Gaenslen FJ. Sacroiliac arthrodesis: Indications, author's technic and end-results. JAMA. 1997; 89: 63-68; 2031-2035. [ Links ]
46. Waisbrod H, Krainick JU, Gerbershagen HU. Sacroiliac joint arthrodesis for chronic lower back pain. Arch Orthop Surg. 1987; 106: 238-240. [ Links ]
![]() Dirección para correspondencia:
Dirección para correspondencia:
Av. México-Xochimilco 289,
Col. Arenal de Guadalupe,
CP 011400, delegación Tlalpan,
México DF,
Tel. 59991000 Ext. 11226,
Fax 5271 6138,
gisibyg@yahoo.com.mx
Financiación: Ninguna
Conflictos de interés: No declarados
Recibido: 20/03/2008
Aceptado: 20/04/2008